9. Застосування бактеріостатиків
Останнім часом значно зріс інтерес дослідників і виробників до біотехнологічних методів модифікації м'ясної сировини, заснованих на індивідуальних властивостях мікроорганізмів. Цілеспрямоване використання мікроорганізмів сприяє одержанню стабільної якості готового продукту. Технологічна дія мікроорганізмів пов'язана з утворенням специфічних біологічно активних компонентів: органічних кислот, бактеріоцинів, ферментів, вітамінів й ін., що сприяє поліпшенню санітарно-мікробіологічних, органолептичних показників готового продукту, а також дозволяє інтенсифікувати виробничий процес.
Як стартові культури в основному використовуються денітрифікуючі коки й гомоферментативні молочнокислі бактерії.
Завдяки молочнокислим бактеріям відбувається здійснення біохімічних перетворень основних компонентів м'яса з утворенням з'єднань, що обумовлюють смак й аромат, консистенцію. Разом із цим відбуваються зміни фізико-хімічних параметрів м'ясного фаршу в напрямку, несприятливому для розвитку мікробів, здатних викликати псування м'яса; придушення розвитку небажаної й патогенної мікрофлори шляхом утворення різних речовин, що володіють антимікробною дією.
Зростаюча поінформованість про потенційну шкоду консервантів для здоров'я сприяє проведенню досліджень по визначенню можливості використання молочнокислих мікроорганізмів як компонентів, що зменшують число небажаних мікроорганізмів, а також їхніх функціональних метаболітів у якості біоконсервантів.
Один з можливих способів дії молочнокислих мікроорганізмів, результатом якого є придушення небажаної й становлення певної мікрофлори, це виділення антибактеріальних речовин, таких як органічні кислоти, діоксид вуглецю, пероксид водню, диацетил, а також бактеріоцинів. Цим пояснюється їх комплексна антимікробна дія, що дає можливість використовувати їх як природні консерванти продуктів харчування. Бактеріоцини педіококів, педіоцини, активні проти Listeria і мають значний потенціал у якості біоконсерванту для м'ясної промисловості.
На продукцію бактеріоцинів бактеріями впливають склад поживного, середовища, рН, температура, час інкубації продуцента, а також достатня кількість живильних речовин, необхідних для клітинного й енергетичного обміну лактобактерій, основними з яких є вуглеводи й фосфати. Актуальна розробка оптимального за складом середовища з паралельним зниженням його вартості. Для стабільного синтезу бактеріоцинів молочнокислими бактеріями потрібні середовища складного складу, що забезпечують клітини необхідними компонентами. Створення умов, що сприяють нагромадженню клітинної маси, забезпечує найбільшу продукцію бактеріоцинів.
Багато бактерій синтезують антибіотичні речовини білково-пептидної природи, що вбивають родинні види або штами, або гальмують їх ріст, або мають більш широкий спектр антибактеріальної дії. Ці речовини з досить специфічною дією одержали назву бактеріоцинів, біосинтез яких кодується, найчастіше, особливими плазмідами й відбувається в більшості випадків на рибосомах.
Бактеріоциногенія – біологічний феномен, широко розповсюджений у природі й пов'язаний з антагонізмом у бактерій. Дослідження останніх років дозволили виділити в самостійну категорію явищ антагоністичну активність мікроорганізмів, що характеризується синтезом білковоподібних антибактеріальних речовин з обмеженим діапазоном активності.
Утворення бактеріоцинів установлене в наступних родів грампозитивних бактерій: Bacillus, Clostridium, Strеptococcus, Leuconostoc, Lactobacillus,Staphylococcus, Micrococcus, Corynebacterium, Mycobacterium, Sarcina, а також в Streptomyces.
Бактеріоцини за молекулярною вагою, структурі, чутливості до тепла розділяють на чотири групи.
I – лантибіотики, що складаються з модифікованих амінокислот (лантионін, β-метиллантионін, дегідробутирин і дегідроаланін). Ia – включає нізин, що складається з катіоноактивних і гідрофобних пептидів, що утворюють пори в цитоплазматичних мембранах. Ib представлений кулястими (компактна, згорнута молекулярна структура) пептидами, що не мають негативного заряду або заряду взагалі.
II – нелантибіотики, немодифіковані термостабільні пептиди з молекулярною вагою не більше 5 кДа. IIa – антилистеріальні пептиди. Відповідно до загальноприйнятої класифікації, клас IIa включає педіоцин подібні пептиди, активні проти Listeria, що складаються із двох модулів: гідрофільного консервативного N-кінцевого (Tyr-Gly-Asn-Gly-Val і двома цистеїнами, що формують містки S-S) і більш варіабельного гідрофобного С-кінцевого. IIb – бактеріоцини, що складаються із двох пептидів, IIc – тіолактивовані пептиди.
III – термолабільні пептиди з молекулярною вагою більше 30 кДа.
IV – комплексні бактеріоцини, гетерогенні протеїни, що мають у своєму складі небілкову частину (вуглевод або ліпід), необхідну для біологічної активності.
Мішенню для багатьох низькомолекулярних катіонних пептидів (клас бактеріоцинів Iа – лантибіотики, що включає нізин) є цитоплазматична мембрана чутливих клітин. Катіонні пептиди формують пори в цитоплазматичній мембрані, руйнуючи протонрушійну силу (ПРС) клітини-мішені. ПРС, що складається з хімічного компонента (градієнт рН – ΔрН) і електричного компонента (мембранний потенціал Δψ), здійснює синтез АТФ, акумулювання іонів й інших метаболітів через транспортну систему в мембрані, керовану також протонрушійною силою.
Колапс ПРС, що викликається дією бактеріоцинів, є причиною підвищення проникності мембрани й втрати низькомолекулярних компонентів розміром до 0,5 кДа (АТФ, амінокислоти, іони) через неї, що призводить до загибелі клітини. Це добре видно на прикладі втрати іонів К+ бактеріальною клітиною (рис. 45).
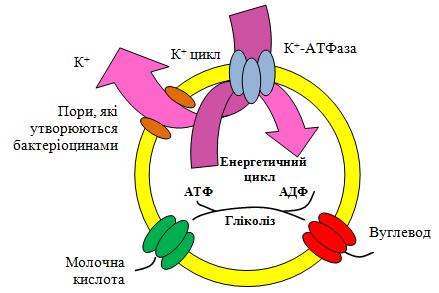
Рис. 45. Эффлюкс іонів калію за участю К+-АТФази.
Перенос іонів калію через пори в клітинних мембранах у нормі здійснюється за участю ферменту К+-АТФази. Фермент К+-АТФаза гідролізує молекули АТФ і використовує енергію, що звільняється при гідролізі АТФ, для переносу іонів калію через клітинну мембрану. У результаті мікробна клітина гине від енергетичного виснаження.
Бактеріоцини неоднорідні за механізмом дії. Ряд авторів вважає, що механізм дії бактеріоцинів з лактококів – це утворення пор у цитоплазматичній мембрані чутливих клітин. Однак, Laсtococcus lactis утворює два класи бактеріоцинів: лантибіотики (нізин й ін.), пептиди, що містять незвичайні амінокислоти (лантионін й ін.), і клас термостійких коротких поліпептидів, що не містять лантионіну. Різниця в механізмі дії цих двох класів лактококових бактеріоцинів полягає в тому, що механізм дії нізина не допускає рецептора, нізин вбудовується у внутрішню мембрану, утворюючи іонні канали або пори. Нелантибіотичні бактеріоцини – диплококцин, лактострепцин і лактококцини – утворюють пори, які взаємодіють зі специфічним рецептором.
Здатність бактерій продукувати бактеріоцини визначається наявністю в клітині бактеріоциногенних факторів, певних генетичних детермінантів. Ще в 70-х роках висловлювалася думка, що здатність продукувати, наприклад, коліцини визначається наявністю в бактерій продуцентів специфічних генетичних детермінантів, так званих колициногенних факторів.
Відомо, що бактеріоцини, що продукуються молочнокислими бактеріями й належать до сімейства педіоцинів, складаються із двох модулів: гідрофільного консервативного N-кінцевого й більш варіабельного гідрофобного С-кінцевого. Застосування методів генної інженерії дозволило сконструювати чотири нових гібридних бактеріоцини, що володіють біологічною активністю й специфічністю відносно різних штамів бактерій, подібної зі специфічністю батьківського бактеріоцину, від якого взятий С-кінцевий фрагмент. Зроблено висновок, що в педіоциноподібних бактеріоцинів специфічність до клітинки-мішені визначається С-кінцевим фрагментом.
При розгляді екологічної ролі бактеріоцинів відзначають, що бактеріоцини відіграють більшу роль у природних бактеріальних співтовариствах. Синтез цих речовин має значення для конкуренції усередині популяції й між ними.
У природних умовах бактеріоциногенія може бути одним із факторів, що впливають на формування мікробного ценозу. Тому великий інтерес представляє з'ясування значення цього явища для розвитку популяції. У бактеріоциногенних популяцій сумарна захисна активність проявляється в придушенні розвитку інших бактерій, що володіють подібними харчовими потребами (родинні види мікроорганізмів). Це придушення забезпечується бактеріоцином, що продукує окремі клітини цієї популяції. Таким чином, бактеріоциногенні бактерії мають важливу селективну перевагу в умовах мікробних асоціацій, що природно складаються в процесі еволюції.
Молочнокислі бактерії звичайно використаються як стартові культури у ферментованих продуктах. Тому дослідження, спрямовані на вивчення використання стартових культур, що синтезують бактеріоцини, є перспективними.
Молочнокислі бактерії утворюють широкий спектр бактеріоцинів: курвацин, диацетин, лактококцин, ацидоцин, лактоцин, плантацин, плантарицин й ін. Бактеріоцини молочнокислих бактерій розділяють на дві групи. Представники першої групи характеризуються вузьким спектром антибактеріальної дії – викликають загибель організмів, близьких до організму-продуцента. У цю групу входять лактоцин В і F-27, аміловорин, педіоцин N5P, теpмофілін А, курвацин А, аміловорин L471, ентерококцин. Бактеріоцини, що належать до другої групи, інгібують ріст багатьох видів грампозитивних мікроорганізмів, у тому числі Listeria monocytogenes, Clostridium botulinum, Clostridium sporogenes, Staphylococcus aureus, Pediococcus acidilactici, Bacillusspp., Enterococcus faecalis. Перераховані бактерії викликають псування харчових продуктів, серед них є й патогенні види. До бактеріоцинів другої групи належать педіоцин А, ацидоцин В, диацетин В-1, курвацин FS47, лактицин 3147, плантарицин С, ентерококцини, саліварцин, нізин, саркацин 674, мутацин. Показано, що більша частина цих бактеріоцинів не токсична й не імуногенна.
Ряд властивостей бактеріоцинів (інактивація протеїназами й стійкість до нагрівання) підтверджують їх білкову або пептидну природу. Вивчення умов утворення бактеріоцинів представниками деяких молочнокислих бактерій Lactococcus lactis, Pediococcus acidilactici, Leuconostoc carnosum,Leuconostoc mesenteroides показало, що умови, що сприяють нагромадженню клітинної маси, забезпечують найбільшу продукцію цих з'єднань.
Бактеріоцини, що продукуються групою молочнокислих бактерій, використовуються в складі заквасочної культури в різних харчових виробництвах як природні консерванти для харчових продуктів. Бактеріоцин, що утвориться, забезпечує домінування потрібної мікрофлори й придушення сторонньої мікрофлори, що забезпечує безпечне протікання мікробіологічних процесів.
Для ефективного застосування бактеріоцинів у харчовій промисловості необхідно оптимізувати продукування бактеріоцинів бактеріями, підвищити активність і стабільність цих з'єднань, цілеспрямовано одержувати бактеріоцини із заданими властивостями. Молочнокислі бактерії з родів Lactococcus,Lactobacillus, Pediococcus, Leuconostoc, утворюють антибактеріальні речовини, зокрема бактеріоцини, які можуть використовуватися для консервації їжі.
Здатність продукувати бактеріоцин і стійкість до гомологічного бактеріоцину (імунітет) – це основні ознаки, що відрізняють бактеріоциногенні мікроорганізми від небактеріоциногенних.
В останні п'ятнадцять років у ряді європейських країн (Нідерланди, Ірландія, Великобританія, Франція й ін.), США і Японії проводяться глибокі наукові дослідження з одержання й практичного використання бактеріоцинів для консервування сировини й різних продуктів харчування.
У процесі ферментації й сушіння м'ясних продуктів може відбуватися ріст таких патогенних мікроорганізмів, як Listeria monocytogenes, тому що ці бактерії здатні виживати в кислому середовищі і є стійкими до значної кількості солі й нітриту.
Листерії з недавнього часу віднесені до санітарно-показових мікроорганізмів. Для контролю росту Listeria monocytogenes у м'ясних продуктах дослідники пропонують використовувати бактеріоцини. Листерії, що розвиваються в харчових продуктах і призводять до їхнього псування, придушуються наступними бактеріоцинами: курвацином FS47, диацетином В-1, педіоцином, сакацином, ентерококцинами. Інгібуючий ефект визначали в бульйоні, у стерильному продукті, у процесі готування сосисок.
Молочнокислі бактерії, виділені з м'яса й м'ясних виробів, - кращі мікроорганізми для мікробіологічної безпеки цих харчових продуктів, тому що вони добре пристосовані до умов у м'ясі й тому більш конкурентоздатні, ніж молочнокислі бактерії з інших джерел.
Антилистеріальним ефектом також володіє бактеріоцин педіоцин, який продукується штамом Pediococcus acidilactici PAC. Було встановлено, що в процесі ферментації м'ясних продуктів рівень Listeria monocytogenes знижується. Отже, застосування штаму Pediococcus acidilactici PAC, що продукує бактеріоцин, у ковбасному виробництві дуже перспективно.
Бактеріоцини використовуються в консервуванні, як у вигляді готових препаратів, так й у вигляді захисних культур мікроорганізмів, що синтезують ці з'єднання безпосередньо в харчовому продукті.
Самим вивченим бактеріоцином у цей час є нізин, відкритий в 1928 р, синтезований культурою Streptococcus lactis. Головним достоїнством нізина є його виражена інгібуюча дія на більшість клостридій, грампозитивних термостійких бактерій та їх спор, що особливо важливо при виробництві консервів.
Однак нізин має дуже вузький спектр антимікробної дії. Грамнегативні бактерії, дріжджі й гриби нізином не пригнічуються, а, навпаки, швидко руйнують нізин. Стійкі до цього бактеріоцину й листерії, особливо Listeria monocytogenes. Крім того, використання нізина для стабілізації властивостей фаршевих м'ясопродуктів не забезпечує їх надійного антимікробного захисту.
Антимікробний потенціал молочнокислих бактерій складається не тільки з нізина й органічних кислот, але й деяких специфічних з'єднань. Серед метаболітів штаму Lactobacillus reuteri LTH2584 виявлено, виділено й очищено до гомогенного стану з'єднання з антимікробними властивостями – реутерициклін. Ця речовина справляє інгібуючу дія відносно бактерій Lactobacillus spp., Bacillus subtilis. B. cereus, Enterococcus faecalis, Staphylococcus aureus й Listeria innocua; у відношенні L. sanfranciscensis, S. aureus й B. subtilis проявляє бактерицидну дію, на ріст грамнегативних бактерій не робить ніякого впливу.
Широкий спектр бактеріоцинів, що продукуються молочнокислими бактеріями, служить підставою для ідентифікації цих з'єднань і визначенню областей їхнього використання. Зокрема, культура Lactobacillus plantarum ST 31, виділена із закваски, продукує з'єднання з інгібуючою активністю, позначене як плантарицин ST 31. Плантарицин ST 31, як й інший антимікробний пептид педіоцин РА-1, може знайти застосування в харчовій промисловості в якості біоконсервантів. Однак зберігання при температурі вище 4 °С викликає швидку втрату їхньої активності.
Наведені дані свідчать, що молочнокислі бактерії можуть знайти широке застосування в біоконсервуванні харчових продуктів, тому що вони є природними представниками мікрофлори людського організму, і вся історія вивчення лактобацил свідчить про їхню безпеку. Ці мікроорганізми пропонують використати й у якості пробіотиків, що сприятливо впливають на здоров'я людей.
Молочнокислі бактерії, розвиваючись у природних і виробничих субстратах, вступають у складні взаємини з іншими мікроорганізмами. Характер із взаємин залежить від багатьох факторів. Істотну роль грає видова приналежність мікроорганізмів, що спільно розвиваються. Спрямованість взаємин більшою мірою визначається умовами середовища перебування й може змінюватися в процесі розвитку мікроорганізмів.
Рід Pediococcus представлений грампозитивними, неспороутворюючими, нерухомими коками, що розташовуються купками, тетрадами, парами, одинично; іноді згадують і про утворення коротких ланцюжків, що складаються з 4…6 клітин.
Педіококи – мікроаерофіли або анаероби, часто потребують присутності СО2 для забезпечення задовільного росту. Вони, як правило, не утворюють каталазу, не відновлюють нітрати в нітрити, не розріджують желатин. Рідко підкисляють, сквашують молоко й відновлюють у ньому лакмус. Деякі штами продукують слиз із сахарози. Педіококи викликають гомоферментативне молочнокисле бродіння, утворюючи при цьому до 1% оптично неактивної (іноді L+) молочної кислоти, а також інші продукти – ацетальдегід, диацетил, ацетоїн, сліди 2 або 3-метил-1-бутанола, ізобутанолу, рН середовища при цьому знижується до 3,7.
Морфологію клітин (через 24 й 48 год) і форму колоній (через 1, 2, 7 доби інкубації) вивчають за одним із використовуваних для виділення й культивування педіококів середовищ, наприклад, агаризованому або рідкому середовищу з томатним соком. Звичайна температура інкубації посівів +30 °С; для P. damnosus +22 °С.
Від представників роду Streptococcus педіококи відрізняють за морфологією. На противагу мікрококам, вони не ростуть на простих середовищах (живильний агар без відповідного вуглеводу), не засвоюють солі амонію як єдине джерело азоту, не відновлюють нітрати до нітритів або N2, не розріджують желатин, не ростуть у середовищах із рН 9,0, підкислюють бульйон із глюкозою до рН 4,5 і нижче. Ріст при різних температурах, солестійкість, здатність рости при різних рН можна досліджувати на середовищі MRS. Потребу в кисні визначають за інтенсивністю росту культур у бульйоні з томатним соком в аеробних або анаеробних умовах в атмосфері 95% Н2 й 5% СО2. Візуально відзначають ріст після інкубації протягом 24 або 72 год (для повільно зростаючих штамів).
