3.5. Виробництво інфузійних розчинів
Інфузійні розчини є найскладнішою групою лікарських засобів для парентерального застосування. До них відносяться фізіологічні розчини, які за складом розчинених речовин здатні підтримувати життєдіяльність клітин і органів, не викликаючи істотних зрушень фізіологічної рівноваги в організмі.
Для виготовлення лікарських засобів для парентерального застосування використовують допоміжні речовини, які забезпечують ізотоніч- ність препаратів щодо крові, регулюють рН, поліпшують розчинність діючих речовин, запобігають розкладанню, забезпечують відповідні антимікробні властивості препарату. Ці речовини у використовуваних концентраціях не повинні негативно впливати на дію лікарського засобу, бути нетоксичними і не викликати небажане місцеве подразнення.
Як допоміжні речовини використовують кислоти аскорбінову, хло- роводневу, винну, лимонну, оцтову, натрію карбонат, натрію гідроксид, натрію або калію сульфат, бісульфіт або метабісульфіт, натрію тіосульфат, натрію цитрат, натрію фосфат одно- і двозаміщений, натрію хлорид, ніпагін, ніпазол, динатрієву сіль етилендіамінтетраоцтової кислоти, спирт полівініловий, хлорбутанол, крезол, фенол тощо.
Кількість деяких допоміжних речовин, якщо немає інших вказівок у приватних статтях, не повинна перевищувати таких концентрацій: для речовин типу хлорбутанолу, крезолу, фенолу - до 0,5 %, сірчистого ангідриду чи еквівалентних кількостей калію або натрію сульфіту, бісульфіту або метабісульфіту - до 0,2%.
У медичній практиці застосовується велика кількість інфузійних розчинів. За функціональним призначенням інфузійні розчини підрозділяють на групи відповідно спрямованості їх дії.
1. Регулятори водно-сольовош балансу і кислотно-основного стану: сольові розчини, осмодіуретики. Розчини здійснюють корекцію складу крові при зневодненні, викликаному діареєю, набряках мозку, токсикозі.
2. І емодинамічні (протишокові) розчини. Призначення для лікування шоку різного походження і відновлення порушень гемодинаміки, зокрема мікроциркуляції, при використанні апаратів штучного кровообігу для розведення крові під час операцій і т. п. Дезінтоксикаційні розчини, що сприяють виведенню токсинів при інтоксикаціях різної етіології.
3. Препарати для парентерального живлення. Служать для забезпечення енергетичних ресурсів організму, доставки поживних речовин до органів і тканин.
4. Переносники кисню. Відновлюють дихальну функцію крові.
5. Комплексні розчини, що мають широкий діапазон дії і можуть комбінувати декілька вищеперелічених груп інфузійних розчинів.
За складом і особливостями застосування інфузійні розчини можна об’єднати в наступні групи:
1. Плазмозамінні і дезінтоксикаційні розчини. Дана група представлена найбільш широким асортиментом препаратів, що включає:
Препарати для корекції об 'єму, складу і деяких функцій циркулюючої крові:
- препарати природного походження - препарати крові (цілісна кров, нативна, суха, заморожена плазма, альбумін); компоненти крові (еритроцитарна і тромбоцитарна маса, лейкоцитарний концентрат, імунологічно активні, гемостатичні препарати);
- синтетичні колоїди (високо-, середньо- і низькомолекулярні), що здатні утримувати воду.
Препарати для підтримки і відновлення об 'єму і складу внутрігиньо-і позаклітинної рідини:
- розчини глюкози (ізотонічні і гіпертонічні); розчини солей (гіпертонічні та ізотонічні).
2. Субстратвмісні препарати, що застосовуються для парентерального живлення:
- препарати - джерела амінокислот;
- препарати — джерела жирних кислот;
- препарати - джерела вуглеводів.
Інфузійні лікарські засоби можна класифікувати залежно від типу лікарської форми, в якій вони існують:
- емульсії;
- концентрати для внутрішньовенних інфузій,
- порошки та ліофілізовані лікарські форми для внутрішньовенних інфузій;
- інфузійні лікарські препарати, приготовлені методом заморожування;
- розчини для внутрішньовенних інфузій.
НТД на інфузійні лікарські засоби включає наступні розділи: опис, достовірність, рН, прозорість, кольоровість, механічні включення, стерильність, пірогенність, токсичність, осмолярність, рєактогенність (для високомолекулярних розчинів), об’єм наповнення, середня маса вмісту (для порошків), однорідність дозування (для порошків), специфічні домішки, супутні або сторонні домішки, важкі метали, кількісний вміст, маркування і пакування.
Розчини для внутрішньовенних інфузій
Розчини для внутрішньовенних інфузій призначені переважно для застосування у великих об’ємах. Внутрішньовенні інфузійні розчини не містять антимікробних консервантів і у відповідних умовах спостереження повинні бути прозорими і практично вільними від механічних частинок.
Одним з найпоширеніших розчинників, шо застосовуються в приготуванні інфузійних розчинів, є вода для ін’єкцій.
До одного з найпоширеніших інфузійних розчинів відноситься розчин натрію хлориду ізотонічний 0,9 %, що ізотонічний плазмі крові і тому називається фізіологічним.
Номенклатура сольових розчинів, що випускаються підприємствами України, включає також ряд багатокомпонентних препаратів електролітів: «Дісоль», «Трісоль», «Ацесоль», «Хлосоль», «Квінтасоль», розчин Рінгера.
Провідне місце в номенклатурі інфузійних розчинів займає розчин глюкози 5, 10, 20 і 40 %.
Як парентеральне живлення в медичній практиці знайшли широке застосування інфузійні розчини на основі декстрану, такі як «Реополі- глюкін», «Поліглюкін».
До поширених інфузійних розчинів, що підтримують колоїдний осмотичний тиск на рівні аналогічного показника крові, належать препарати на основі полівінілпіролідону (з молекулярною масою 8000±2000) - «Неогемодез» і «Гемодез Н».
Для парентерального живлення застосовуються інфузійні розчини, які є гідролізатами, що отримуються з білків крові великої рогатої худоби або людини, казеїну та інших білків, а також такі, що є розчинами «чистих» амінокислот
Емульсії для внутрішньовеншіх інфузій
Емульсії для внутрішньовенних інфузій є однорідною на вигляд лікарською формою, що складається із взаємно нерозчинних тонко- диспергованих рідин, призначених для парентерального застосування. Емульсії для внутрішньовенних інфузій вимагають тонкого подрібнення дисперсної фази для уникнення емболії при введенні емульсії в кров’яне русло і не повинні виявляти ознак розшарування.
Концентрати для внутрішньовенних інфузій
Інфузійні розчини лікарських засобів випускаються як у готових до застосування формах, призначених для внутрішньовенних вливань без попереднього розбавлення в інфузійних середовищах, так і у формі концентрованих розчинів для інфузій, що містять лікарські речовини в малому об’ємі носія.
Концентрати для внутрішньовенних інфузій є стерильними розчинами, призначеними для інфузій після розведення. Концентрати розводять до вказаного об’єму відповідним розчинником перед застосуванням. Після розведення отриманий розчин повинен відповідати вимогам, що висуваються до інфузійних лікарських засобів.
Однією з додаткових вимог до концентратів для інфузій є сумісність їх з відповідними розчинами, що використовуються для розведення концентратів, стабільність після розбавлення і можливість внутрішньовенного введення.
Як розчинники концентратів для внутрішньовенних інфузій застосовуються в першу чергу сольові розчини і низькоконцентровані (5 %
і 10 %) розчини глюкози, а також, у ряді випадків, інфузійні розчини інших груп, зокрема, білкові розчини.
Порошки та ліофілізовані лікарські форми для внутрішньовенних інфузій
Порошки для внутрішньовенних інфузій являють собою тверді стерильні речовини, поміщені в контейнер. При струшуванні з вказаним об’ємом відповідної стерильної рідини вони швидко утворюють прозорий, вільний від механічних частинок розчин. Після розчинення вони повинні відповідати вимогам, що висуваються до внутрішньовенних інфузійних лікарських засобів.
Перспективною технологією отримання стабільних інфузійних розчинів є ліофілізація, що набула широкого розповсюдження як метод стабілізації речовин, що легко руйнуються. За цим методом стерильний водний розчин лікарської речовини заморожують у стерильному контейнері, лід і зв’язану воду в асептичних умовах видаляють сублімацією і вакуумною сушкою. Сушку заморожуванням можна проводити в готовій упаковці (флаконі, ампулі зі скла або пластику); можна проводити заморожування у балк-формі з подальшим розподілом ліофілізату. При розбавленні ліофілізатів водою отримують інфузійні концентровані розчини, що підлягають розведенню адекватними інфу- зійними ссредовищами-носіями. При ліофілізації знижується рівень забруднення і підвищується якість розчину.
Технологія виробництва інфузійних лікарських засобів
Виробництво розчинів для інфузій здійснюється в приміщеннях класів чистоти А, В, С, Б повітряного середовища.
Необхідний клас чистоти забезпечується за рахунок стерильної вентиляції, застосування установок - очищувачів повітря, створення необхідної кратності повітрообміну, спеціальної підготовки приміщень, устаткування, застосування бактерицидних ламп і підготовки персоналу.
Кожна технологічна операція процесу виробництва стерильних розчинів для інфузій вимагає відповідної чистоти повітря.
До приміщень класу А відносяться локальні зони для проведення технологічних операцій, що вимагають наймінімальнішого ризику забруднення: змішування в асептичних умовах, стерильної фільтрації розчину, наповнення первинної упаковки (флакони, пакети та ін.), герметизації первинної упаковки, збірки стерилізуючих фільтрів, вивантаження стерильних закупорювальних засобів. Умови приміщень класу А передбачають наявність ламінарного потоку повітря з однорідною швидкістю 0,45 м/с+20 %.
Приміщення класу В є навколишнім середовищем для зони класу А у випадках приготування і наповнення в асептичних умовах.
Приміщення класів С і D включають чисті юип для проведення технологічних операцій, що допускають підвищений рігшк іабрудпси- ия при виробництві інфузійної продукції, яка підлягає термічній стерилізації в кінцевій упаковці (приміщення, в яких здійснюється підготовка первинної упаковки і закупорювальних засобів, приготування і фільтрація розчинів, наповнення первинної упаковки, її герметизація і стерилізація продукції в первинній упаковці).
Для попередження мікробної контамінації і забруднення механічними частинками при виробництві інфузійних препаратів передбачаються технологічні і санітарні способи підготовки вентиляційного повітря виробничих приміщень, технологічного устаткування та інвентарю, персоналу і технологічного одягу Очищення повітря, що подається в приміщення А, В і С класів чистоти, повинне бути триступінчастим. На першому ступені застосовуються чарункові фільтри типу ФЯВ або ФЯМ, на другому - сухі рулонні фільтри типу ФРП, на третьому - чарункові фільтри типу ФЯЛ, ЛАЙК, комбіновані фільтри типу 4 Ф або фільтри типу НЕРА або ULPA. Оптимальною для досягнення необхідного класу чистоти є система розміщення фільтрів, в якій фільтри НЕРА сполучені трубопроводами з центральною системою повітрообміну.
У приміщеннях класу чистоти А горизонтальні або вертикальні ламінарні потоки стерильного повітря у всьому об’ємі приміщень створює спеціальне устаткування.
Відповідно до вимог GMP, що висуваються до виробничих приміщень, всі поверхні повинні бути гладенькими, непроникними і непо- шкодженими, щоб звести до мінімуму утворення і накопичення пилу та мікроорганізмів, а також забезпечувати можливість багатократного застосування очищаючих і дезінфікуючих засобів. Покриття підлоги повинне бути не слизьким, стійким до стирання і мати щільну структуру
Під підготовкою виробничих приміщень до роботи розуміють комплекс заходів, що складається з вологого прибирання, дезінфекції та УФ-опромінення, направлених на досягнення відповідного класу чистоти приміщень.
За умовами GMP ВООЗ, для виробництва стерильної лікарської продукції слід використовувати устаткування, яке можна ефективно стерилізувати парою, сухим жаром або іншими способами.
Підготовка тари і закупорювальних засобів
Підготовка первинної упаковки інфузійних лікарських засобів включає ряд операцій: розтарювання, перегляд і відбраковку, набір у касети (за необхідності), миття, сушіння, стерилізацію. Кожна з них або групи операцій повинні проводитися в приміщеннях певного класу чистоти, обумовленого особливостями виробництва конкретного препарату (див. Додаток 2).
Підготовки флаконів
Миття зовнішньої і внутрішньої поверхні флаконів здійснюється в основному із застосуванням шприцевого або ультразвукового методу або їх комбінацій.
Метод шприцювання оснований на обробці флаконів під тиском профільтрованими водою очищеною, парою, повітрям при положенні флакона горловиною вниз.
Ультразвуковий спосіб миття оснований на використанні коливань, що випромінюються магнітострикційними перетворювачами, вмонтованими у дно або кришку апарата. При даному способі миття флакони занурені у воду на певній відстані від випромінювачів.
Ефективнішим є контактно-ультразвуковий спосіб очищення за рахунок безпосереднього контакту стінок флакона з джерелом коливань. При цьому ультразвукові коливання збуджуються у самому виробі, що очищається, який стає випромінювачем, і очищення поверхні здійснюється як за рахунок специфічних ефектів, що виникають в рідині (імпульси тиску при захлопуванні кавітаційних порожнин), так і за рахунок механічних коливань самого флакона.
У промислових умовах миття флаконів здійснюється на типовому устаткуванні вітчизняного виробництва (наприклад, лінія підготовки флаконів АЛВ виробництва Маріупольського ЗТО) або на імпортних.
Обполіскування флаконів проводять водою для ін’єкцій, профільтрованою через мембранний фільтр з порами розміром не більше 5,0 мкм.
Після миття флакони за допомогою передавального пристрою надходять на стерилізацію. На цьому етапі використовуються сушильно-стерилі- заційні установки тунельного типу, де флакони проходять три зони: нагрів до температури стерилізації, витримка при цій температурі протягом заданого часу і охолоджування. У всі зони тунеля подається профільтроване через фільтр тонкого очищення стерильне повітря в ламінарному потоці. Температура стерилізації в зоні повинна підтримуватися в межах 315±35 °С, залежно від цього тривалість стерилізації складає від 5 до ЗО хвилин.
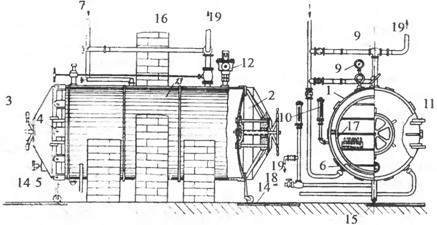
Прикладом використовуваного устаткування для стерилізації може служити тунель сушильної стерилізації (камера Крупіна, Росія (рис. 3.3)); установка сушильної стерилізації LAS (Данія); тунельний стерилізатор «Пірокленз» (Голландія) та ін.
Підготовка закупорювальних засобів
Для підготовки пробок і ковпачків у виробничих умовах необхідно використовувати поліфункціональне устаткування з програмним управлінням, що дозволяє здійснювати всі операції в одному апараті.
Початковою стадією підготовки пробок і ковпачків є перегляд і обробка пробок на відповідність вимогам НТД, які проводяться з метою виключення вторинної контамінації мікроорганізмами або механічними включеннями після миття. Для перегляду закупорювальних засобів повинні бути спеціальні закупорювальні столи, обладнані джерелом денного світла.
|
Рис. 3.3. Стерилізаційна камера Крупіна. 1 - корпус; 2 - кришка; 3 - штурвал, 4 - пази; 5 - повітряний клапан; 6 - зміївик; 7 - трубка; 8 - ежектор; 9 - манометр; 10 - термометр; 11 - петля кришки; 12 - запобіжний клапан; 13 - теплоізоляція; 14 - рейки для відводу матеріалу; 15 - рейки для відводу кришки; 16 - стінка; 17 - матеріал; 18, 19 - труби для виходу пари |
Миття пробок і ковпачків включає декілька операцій почергово!' обробки миючими розчинами і обполіскування.
НТД регламентує наступну послідовність обробки пробок: відмивання гумової крихти й інших механічних забруднень, миття в розчині миючого засобу, дозволено до застосування, кип’ятіння в розчині натра їдкого, соди кальцинованої або тринатрійфосфату, кип’ятіння в розчині кислоти хлороводневої.
Після кожної операції проводять обполіскування пробок проточною водою, потім очищеною.
Останнє обполіскування проводять проточною водою для ін’єкцій, профільтрованою через мембранний фільтр з порами розміром не більше 0,5 мкм.
Допускається проведення силіконування пробок.
Стерилізацію пробок проводять в автоклаві обробкою насиченою парою у воді для ін’єкцій з подальшою сушкою стерильним гарячим повітрям.
Для підготовки пробок використовуються промислові пральні машини і казани (для кип'ятіння пробок).
Послідовність обробки ковпачків включає миття ковпачків в розчині миючого засобу, обполіскування проточною водою питною, кип’ятіння ковпачків у воді очищеній або, при необхідності, в розчині миючого засобу або тринатрійфосфату, обполіскування водою очищеною. Останнє обполіскування проводять проточною водою для ін’єкцій, профільтрованою через мембранний фільтр з порами розміром не більше 5,0 мкм.
Стерилізацію ковпачків проводять насиченою парою в автоклаві у воді очищеній або в електростерилізаторі. Сушка ковпачків проводиться стерильним гарячим повітрям. Підготовлені стерильні матеріали первинної упаковки передаються в чисту зону через вмонтований у стіну стерилізатор із двостороннім доступом.
Матеріали первинної упаковки повинні проходити випробування на мікробіологічну чистоту. При виробництві інфузійних лікарських засобів, що не підлягають термічній стерилізації, слід контролювати їх стерильність і при необхідності - пірогенніс гь.
Також матеріали первинної упаковки контролюються на вміст механічних включень.
Приготування інфузійних розчинів
Як витікає з представленої загальної блок-схеми виробництва інфузійних розчинів (див. Додаток 4), основними стадіями виробництва є:
^ підготовка виробництва:
^ підготовка сировини і води для ін’єкцій;
^ підготовка флаконів до наповнення:
^ приготування і фільтрація розчину;
^ наповнення, закупорювання і закатка флаконів;
пакування, маркування готової продукції.
Місткості (реактори), в яких здійснюють приготування розчинів для інфузій, повинні бути скляні, фарфорові, емальовані або із спеціальних сортів сталі, герметично закриватися, бути забезпеченими мішалкою і, у ряді випадків, паронагрівачем. Вони не повинні мати вад, щоб уникнути забруднення розчинів або хімічної дії на них. Всі частини технологічного устаткування, що стикаються з розчинами, повинні бути виготовлені з хімічно стійких матеріалів.
Закриті ємності для вихідних розчинів чи напівпродуктів повинні бути попередньо очищені та простерилізовані; у чистих приміщеннях проводять контроль на наявність частинок у стані спокою, при роботі установок і в процесі виробництва. Застосовують лазерний пристрій для підрахунку частинок.
Будь-який газ (стиснений, природний, інертний), що контактує в ході технологічного процесу з розчинами чи іншою проміжною продукцією, повинен пройти стерилізуючу фільтрацію.
Розчини для інфузій готують за ваго-об’емним принципом, тобто розчинювані речовини беруть по вазі, а розчинника стільки, щоб отримати заданий об’єм розчину.
Для збільшення швидкості розчинення можна змінювати температурний режим, зменшувати в’язкість шляхом зміни гідродинамічних умов і попередньо подрібнювати вихідну речовину. Часто технологічний процес розчинення проводять у реакторах, що мають обігрів парою або охолодження системи водою чи розсолом, і перемішуючий пристрій. Перемішування дозволяє переміщати шари рідини в реакторі, змінюючи різницю концентрацій речовини у розчиннику і замінюючи молекулярну дифузію в рідкому середовищі на конвектний і турбулентний масопсрснос. Інтенсивне перемішування зменшує товщину дифузного межового шару, інтенсивний масоперенос сприяє швидкому завершенню розчинення.
Перемішування в рідкому середовищі здійснюють кількома способами:
^ механічне - за допомогою мішалок різної конструкції;
^ пневматичне — стисненим повітрям або інертним газом з пульсацією чи без неї;
^ гравітаційне — перемішування, основане на різній щільності розчинника і розчину, здійснюється самочинно, наприклад, розчинення відбувається за рахунок циркулюючих потоків різної концентрації;
^ акустичне (ультразвукове) перемішування досягається застосуванням магнітострикційних та гідродинамічних типів рідинних свистків і роторно-пульсаційного апарата. У цьому випадку за рахунок кавітації, механічної дії подрібнюється тверда фаза, що значно прискорює процес розчинення;
^ циркуляційне (перемішування перекачуванням рідини за допомогою насоса з ємності і повертання до неї через розбризкуючий пристрій). Циркуляцію всередині реактора можна створити подаванням пари в рідину через сопло, при цьому одночасно здійснюють нагрівання.
Найбільш поширеним та використовуваним у виробництві при приготуванні інфузійних розчинів є механічне перемішування за допомогою мішалок різної конструкції. Залежно від швидкості обертання вони діляться на тихохідні (0,2-1,3 об/с) та швидкохідні (2-30 об/с). Робочою їх частиною є лопаті різної форми, які кріпляться на валу і приводяться в обертальний рух від електродвигуна через передавальний механізм. За влаштуванням лопатей розрізняють мішалки лопатеві, пропелерні, турбінні та ін. Вони застосовуються для перемішування рідин малої в’язкості і складаються з двох чи більше лопатей і навіть можуть бути багаторядними (багатоярусними), коли для збільшення об’єму перемішуваних шарів на одному валу кріпиться декілька лопатей на різній висоті.
До лопатевих мішалок відносяться мішалки спеціального призначення: якірні, рамні і планетарні.
Якірні мішалки мають форму, що відповідає внутрішній поверхні реактора, і їх діаметр близький до внутрішнього діаметра апарата. Вони служать для перемішування в’язких рідин: при обертанні лопаті постійно очищають стінки і дно апарата. Швидкість обертання невелика і складає 1,3 об/с.
Рамні мішалки, як і якірні, міцні і призначені для перемішування в’язких рідин. Складаються з декількох лопатей, з’єднаних у вигляді рами для перемішування широких, по всій товщині апарата, шарів рідини.
Планетарні мішалки складаються із центральної та бокових, з’єднаних з головною системою, зубчастих передач і мають власне обертання навкруг осі і разом з центральною. Вони забезпечують рівномірне перемішування в’язких і густих рідин.
Пропелерні мішалки мають гвинтоподібно зігнуті лопаті — кут нахилу по довжині від 45° біля маточини до 20° на кінці лопаті, що забезпечує захоплення всіх шарів рідини. Швидкість обертання для в’язких рідин складає 2-8 об/с, а для рухомих - 3-30 об/с.
Турбінні мішалки можуть бути відкритого і закритого типу з плоскими і похилими лопатями. Забезпечують інтенсивне перемішування, створюючи радіальні та осьові потоки рідини.
У ряді випадків приготування розчинів для інфузій супроводжується додатковими операціями: підготовкою сировини (наприклад, прожарення субстанції натрію хлориду) або очищенням розчинів від каламутності, опалесценції або солей важких металів (адсорбцією).
Інфузійні розчини повинні піддаватися стерилізуючій фільтрації.
Після стадії фільтрації наступною є стадія наповнення первинної упаковки інфузійними розчинами, закупорювання флаконів або герметизація полімерних ємностей. Цей процес на фармацевтичних підприємствах частково або повністю автоматизований і здійснюється за допомогою дозуючих установок різної конструкції і продуктивності.
Способи визначення кількості і розміру механічних включень
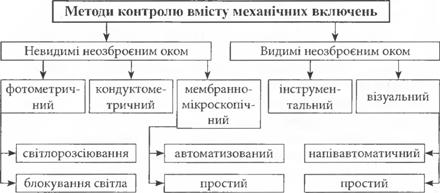
Методи контролю вмісту механічних включень в розчинах дл> ін’єкцій можна розділити на дві групи: виявлення видимих і невидимих неозброєним оком частинок. Прийнято вважати, що до останніх відносяться частинки розміром менше 50 мкм. За характером контролю способи можна розділити на такі, що руйнують чи не руйнують зразки продукції.
Для контролю видимих неозброєним оком частинок використовують два способи візуальний та інструментальний. Звичайний пристрій для візуального контролю складається з екрана і лампи розжарювання або флуоресцентної, з конденсованим або поляризованим світлом. Джерело освітлення може бути розташоване зверху знизу або збоку від контрольного зразка. Цей метод використовується з 60-х років XX століття, у 70—80-ті роки були розроблені напівавтоматичні системи контролю видимих неозброєним оком частинок типу “Беісіепасіег”, “Уі- яотаг” (Німеччина), “Capsulit” (Італія) та ін. Ці системи мають вищу продуктивність, тому що з їх використанням можна проводити більшу кількість механічних маніпуляцій, таких як подача, струшування та відбраковування зразків.
Класпфікацію способів контролю ін’єкційних препаратів за показниками “Вміст механічних включень” можна подати у вигляді схеми:
|
|
Встановлено, що напівавтомати знижують втому очей контролера і забезпечують вищу якість контролю за рахунок застосування лінз із збільшенням у 1,5-2 рази.
Візуальний контроль дозволяє деякою мірою ідентифікувати вигляд і форму частинок, а також розрізняти кульки повітря, що неможливо при інструментальному контролі і може послужити причиною помилки. Оскільки у будь-якому випадку рішення приймає контролер, даний метод аналізу дуже суб'єктивний і залежить від цілого ряду чинників: розміру частинок, ступеня контрасту частинок щодо фону, часу спостереження об’єкта, типу освітлення, збільшення, способу збовтування зразка та індивідуальних характеристик контролера. Ці чинники приводять до значного підвищення показника помилок - до 30 %.
Другий можливий спосіб виявлення видимих неозброєним оком частинок - інструментальний - проводиться при використанні електронню автоматичних приладів типу “Autoscan” (фірма “Lekso”, США), “Сотр- ur” (фірма “Bayer”, Німеччина), “Eisai” (фірма “ Eisai “, Японія) та ін.
З метою виключення помилок у ряді систем передбачається багаторазове спостереження кожного досліджуваного зразка.
Ізотонічні розчини Ізотонічні розчини представляють особливу групу ін’єкційних розчинів, які відрізняються тим, що їх осмотичний тиск рівний осмотичному тиску плазми крові, лімфи або сльозової рідини.
Ізотонічність розчинів, що вводяться в організм, досягається збільшенням кількостей натрію хлориду, глюкози, натрію сульфату та ін.
Для уникнення таких небезпечних ускладнень парентеральногс введення лікарських засобів, як гіпо- та гіперосмолярні стани, порушення згортання крові, утворення тромбів і т.д., останніми роками в розчинах для ін’єкцій визначають показники осмоляльності та осмолярності.
Згідно з визначенням Європейської фармакопеї, осмоляльність (х) - це показник, який дозволяє оцінити сумарний внесок різних розчинених речовин в осмотичний тиск розчину. Осмоляльність виражають в осмолях на кілограм розчинника - осмоль/кг (на практиці зазвичай використовується мосмоль/кг).
У фармакопеях США (USP 23) і Японії приведено визначення осмоляльності (т): це показник, який також дозволяє оцінити сумарний внесок різних розчинених речовин в осмотичний тиск розчину.
Осмоляльність - кількість осмолів на L кг розчинника. Осмоль - співвідношення г/мол маси речовини до частинок або іонів, які утворюються при його розчиненні.
Осмолярність — кількість осмолів на 1 л розчину. Її розраховують за формулою:
![]()
де: концентрація речовини - кількість розчиненої речовини на І л розчину, г;
кількість частинок - кількість частинок або іонів, які утворюються при розчиненні однієї молекули речовини.
Однією з основних вимог до якості парентеральних лікарських препаратів є їх стерильність.
Для стерилізації інфузійних розчинів використовують термічні методи стерилізації, зокрема, стерилізацію парою під тиском в автоклаві, останнім часом застосовується метод стерилізуючої фільтрації.