Вологозв'язувальна здатність м'яса
Вода є природною складовою м'яса і певним чином зв'язана з його елементами, утворюючи стійкі структуровані системи. Форми і міцність зв'язку води із структурними елементами тканин зумовлюють здатність м'яса більш-менш міцно утримувати ту чи іншу кількість вологи. Кількість зв'язаної води та її розподілення за формами і міцністю зв'язку впливає на властивості м'яса, у тому числі на його консистенцію. Оскільки кількісно переважальними компонентами м'яса є м'язова і сполучна тканини, їх водозв'язувальна здатність має найбільше практичне значення. Основний структурний матеріал цих тканин — білкові речовини, властивості й стан яких і, визначає водозв'язувальну здатність м'яса.
М'язова тканина в природному стані містить до 75 % води. Більша її частина (близько 90 %) є у м'язових волокнах, інша — в міжклітинному просторі. У середині волокна вода розподіляється нерівномірно: більша її частина зв'язана з білками міофібрил, менша — у саркоплазмі (в живих тканинах концентрація білків міофібрил 15…20 %, білків саркоплазми 25…30%). Отже, водозв'язувальна здатність м'язової тканини залежить насамперед від стану білків міофібрил, міозину, актину і актоміозину.
У сполучній тканині води міститься менше (57…65 %, а в деяких різновидах, наприклад в ахіллових сухожиллях, лише 50 %). Більша частина води зв'язана з колагеном і еластином. Практичне значення має взаємодія води з колагеном. Тенденція білків до зв'язування води пояснюється здатністю полярних груп білкової молекули до взаємодії з її диполями. До таких груп належать, по-перше, іонізовані (заряджені) групування бокових ланцюгів: -NH3 і СОО-. Взаємодію води з ними називають іонною адсорбцією. По-друге, до них належать неіонізовані (незаряджені) групи бокових ланцюгів: -ОН, -SН, -NH- відповідних амінокислот і пептидних груп головних ланцюгів: -СО-NH-. Взаємодію з ними диполів води називають молекулярною адсорбцією.Вода, що зв'язується всіма переліченими групуваннями, фіксується адсорбцією, тому її називають адсорбованою, а самі групування — гідрофільними центрами.
Число іонізованих груп білка залежно від умов, в яких він перебуває, може змінюватися майже до нуля (ізоелектрична точка білка). Водночас змінюється значення іонної адсорбції. Число неіонізованих полярних груп, як правило, залишається незмінним. Практично незмінним є і значення молекулярної адсорбції. Завдяки цьому зберігається здатність білка зв'язувати певну кількість води і в ізоелектричній точці. Іонна адсорбція характеризується міцнішим іонним зв'язком диполів води із зарядженими групами білка, ніж молекулярна. Велику частину адсорбційно-зв'язаної вологи в тваринних тканинах м'ясопродуктів становить волога, яка утворює сольват-оболонку молекул білкових речовин і гідрофільних колоїдів. Частина адсорбційної вологи входить до складу сольватних оболонок гідрофобних колоїдів.
М'ясо є складним структурним утворенням, тому його вологозв'язувальна здатність залежить також від особливостей структури. У цьому розумінні структура має подвійне значення.
По-перше, низькомолекулярні розчинні речовини, які містить структура тканин (клітинні й міжклітинні мембрани, каркас білкових часточок) створюють у тканинах підвищений осмотичний тиск, сприяють припливу води в тканини. Таку воду називають осмотично зв'язаною.
Осмотично зв'язана волога є вільною в тому розумінні, що вона зумовлює дуже малу енергію зв'язку. Волога поглинається без наділення теплоти і стискання системи. Осмотично зв'язана волога дифундує в середині тканин у вигляді рідини через стінки клітин завдяки різниці концентрацій у середині і зовні клітин.
По-друге, структура тканин відрізняється сильно розвиненою системою пор і капілярів порівняно невеликого радіуса. Воду, що утримується системою капілярів, називають капілярною. Ця частина води міститься в капілярах (порах), середній радіус яких 10-7 м. Капілярна волога переміщується в тканинах як у вигляді рідни так і у вигляді пари. Розрізняють два стани капілярної вологи: стиковий стан, коли вона перебуває у вигляді манжеток (защемлена вода), і канатний стан, коли краплі рідини з'єднуються між собою (защеплені повітрям), утворюючи безперервну рідку плівку, що обволікає дисперсні частини тіла.
Таким чином, слід розрізняти три основні форми зв'язку води з м'ясом: адсорбовану, осмотичну і капілярну. Для кожної форми зв'язку води із структурними елементами характерна своя міцність і свій специфічний вплив на стан м'яса і м'ясопродуктів у процесах переробки і зберігання.
Водозв'язувальна здатність м'яса визначає властивості й поведінку м'яса за різних умов. Вона впливає на водозв'язувальну здатність м'ясопродуктів, вироблених з нього, і отже, на їхні властивості й вихід. Проте цей вплив важко піддається кількісній інтерпретації. Справа у тому, що навіть у межах однієї форми зв'язку її вплив на властивості тканин неоднаковий. Водночас залежно від умов і особливостей технологічного оброблення практичні наслідки змін водозв'язувальної здатності м'яса специфічні.
Під час автолізу м'яса зміна частки адсорбованої вологи призводить до перерозподілу води в ньому, внаслідок чого змінюється частка осмотичної вологи. За певних умов (розморожування, нагрівання м'яса) це впливає на кількість м'ясного соку, що відокремлюється. Тому першочергове значення мають зміни адсорбованої з'язаної вологи.
При заморожуванні або сушінні, коли вода відокремлюється від інших компонентів тканин (кристалізацією або випаровуванням), усі форми зв'язку впливають на хід цих процесів хоча і не однаково. Те саме стосується і обводнення зневодненого м'яса. У ковбасному виробництві має значення не тільки вплив усіх форм зв'язку, а й кількісне розподілення вологи за цими формами. Від цього залежить вихід і якість продукції. Тому з практичного погляду зручніше характеризувати водозв'язувальну здатність м'яса і м'ясопродуктів, керуючись передусім міцністю зв'язку адсорбованої вологи.
Залежно від конкретного значення до міцно зв'язаної вологи належать або більша частина адсорбованої вологи мікрокапілярів, або також частина осмотичної вологи (при сушінні і заморожуванні). До слабкозв'язаної (надлишкової) належить та частина вологи, яка може відокремитися під час технологічного оброблення з негативним впливом на якість і вихід продукту (втрати м'ясного соку при розморожуванні, відтік бульйону при варінні ковбас, тощо).
Знаючи роль форми зв'язку вологи для кожного окремого випадку, можна зумовити зміщення рівноваги у бажаний бік, впливати на здатність складових часточок і структури тканин зв'язувати адсорбовану, капілярну і осмотичну вологу.
Кальцій – природний компонент м'ясної сировини, що перебуває в певних фізіологічних кількостях як усередині м'язового волокна в пов'язаному з білками стані, так й у вільній формі в позаклітинній рідині (табл. 47).
Таблиця 47
Вміст загального й іонізованого кальцію в різних компонентах рецептур м’ясопродуктів
|
Об'єкти дослідження |
рН |
Вміст | ||
|
загального кальцію, мг/100 г |
[Са2+], мМ | |||
|
дослід |
літературні дані |
дослід (дані МГУПБ) | ||
|
Яловичина в/г охолоджена Яловичина в/г розморожена |
5,62 5,65 |
13,5 11,0 |
9…11 |
2,9*10-2 15,4*10-2 |
|
Яловичина 1 г розморожена |
6,12 |
10,5 |
8…9 |
0,8*10-2 |
|
Біле м'ясо куряче |
6,02 |
42,4 |
16…20 |
4,0*10-2 |
|
Червоне м'ясо куряче |
5,61 |
19,4 |
8…10 |
0,4*10-2 |
|
М'ясна маса механічної дообвалки |
7,24 |
29,7 |
29 |
5,0*10-2
|
|
Річкова риба (толстолобик) |
7,38 |
29,8 |
40 |
0,4*10-2 |
|
Морська риба (горбуша) |
5,97 |
53,4 |
48 |
1,1*10-2 |
При житті організмів кальцій виконує регуляторну й сигнальну функції, бере участь у процесі м'язового скорочення. Багато білків, що входять до складу м'ясної сировини досить легко вступають у взаємодію з іонами кальцію.
До кальцій-залежних м'язових білків відносяться міозин, тропонін, кальмодулін, парвальбумін, до кальцій-зв'язуючих – білки плазми (протромбін, фібриноген, фактор X), кістки (остеокальцин), молока (казеїн, α-лактоальбумін), деякі ферменти (трипсин, хемотрипсин, термолізин). Є дані про можливу неферментативну деградацію цитоскелетних білків м'язової тканини під дією іонів кальцію, що забезпечує тендеризацію м'яса.
Більша частина розглянутих білків виконує структуруючу функцію, забезпечує зв'язування води, стабілізацію емульсій, і залежно від концентрації іонів кальцію в м'ясній системі (кальцій може бути додатково введений у технологічному процесі не тільки з водою, але й з кухонною сіллю, у якій його вміст досягає 0,65%), можуть відбуватися істотні зміни в ході колоїдно-хімічних процесів. При надлишкових концентраціях кальцію білкова матриця, що утвориться, надмірно зміцнюється, зменшує кількість гідрофільних центрів, емульсійна здатність падає, у результаті чого консистенція готової продукції стає твердою, водозв’язувальна здатність й, відповідно, вихід знижуються.
Результати досліджень показують, що концентрація іонів кальцію в м'ясних системах, зокрема, у м'ясному фарші, робить істотний і неадекватний вплив як на структурно-механічні властивості, так і на активність води.
У діапазоні концентрації іонів кальцію 30…80 мМ в'язкість системи збільшується (рис. 49), частка міцно зв'язаної вологи зростає. При концентрації 90…110 мМ зміна даних показників носить неадекватний характер, що, як видно, обумовлено трансформацією білкової молекули й перерозподілом хімічних зв'язків у системі: м'язові білки-кальцій-вода.
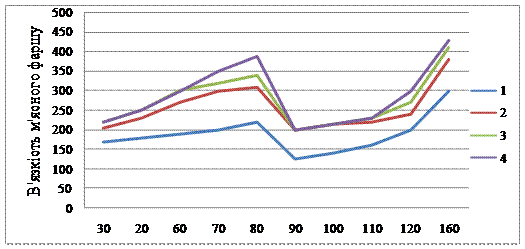
Рис. 49. Вплив концентрації іонів кальцію на в'язкість фаршу, виготовленого з охолодженого м'яса: час витримки м'ясного фаршу, хв: 1 – 5; 2 – 15; 3 – 30; 4 – 60.
Встановлено, що підвищення концентрації іонів Са в м'ясних системах змінює величину активності води:
· при концентрації іонів кальцію 30…80 мМ значення активності води в системах, приготовлених на основі як охолодженого, так і розмороженого м'яса монотонно знижуються;
· при більш високій концентрації іонів кальцію у всіх вивчених зразках фаршу (з охолодженого й розмороженого м'яса, до термообробки й після термообробки) була встановлена різка зміна показника активності, що свідчить про внутрішній перерозподіл води по формах зв'язку вологи в системі.
Вивчення специфіки протікання колоїдно-хімічних реакцій у м'ясних системах при різних концентраціях кальцію може розширити існуючі уявлення про механізм іонотропного структурування харчових систем, а це, у свою чергу, створює передумови до спрямованого регулювання їхніх функціонально-технологічних властивостей й, відповідно, поліпшенню якості готової продукції.
Є відомості про те, що в результаті взаємодії з іоном кальцію (кальцієм-іоном) у білків падає швидкість процесу теплової денатурації, тобто виріб має вигляд сирого, незважаючи на те, що температура в центрі досягла 70±2 °С.
Представлені дані, що характеризують динаміку структурно-механічних властивостей (еластичність і модуль пружності) гелів, приготованих на основі різних видів білкових препаратів, свідчать про досить істотний вплив іонів кальцію на стан отриманих систем.
Широко використовуються в сучасному ковбасному виробництві білкові препарати й препарати, що містять карагінан, також чутливі до іонного складу середовища їхньої гідратації, що відбивається на величині критичної концентрації термотропного гелеутворення, рівні водоутримуючої здатності, тривалості гелеутворення, міцності гелю, ступеня синерезису й т.д.
Із цієї причини при виборі препаратів для конкретних технологічних цілей треба, поряд з перевіркою їх основних функціональних властивостей, проводити оцінку ступеня їх солетолерантності й Са2+-залежності. Якщо буде потреба можна рекомендувати проводити гідратацію Са2+-залежних білкових препаратів (для готування суспензій, гелів й емульсій на їхній основі) у м'якій воді або попередньо вводити в неї фосфати, що осаджують кальцій у вигляді нерозчинних солей.
Слід зазначити, що деякі з харчових гідроколоїдів (наприклад, каппа-карагінан) володіють К+-залежністю й у присутності іонів калію утворюють гелеву сітку, що характеризується підвищеною міцністю й здатністю зв'язувати воду.
