4.2. Сполучна тканина
Структурними елементами сполучної тканини є колагенові, еластинові та ретикулінові волокна з міжклітинною основною речовиною. Сполучна тканина є основою строми та міжклітинної речовини м’язів, входить до складу паренхіматозних органів, підшкірної клітковини, сухожиль, хрящів, кісток, стінок кровоносних, лімфатичних та інших судин, кишок та ін. Вона значною мірою виконує механічні й захисні функції, бере участь у побудові і фізіологічному функціонуванні тканин, сполученні їх між собою, з’єднує окремі тканини зі скелетом тощо.
Колагенові та еластинові волокна зумовлюють жорсткість як сполучної тканини, так і органів, до складу яких входить сполучна тканина (м’язів, легенів та ін.). Залежно від міцності волокон та вмісту міжклітинної основної речовини сполучну тканину поділяють на пухку, щільну і еластинову.
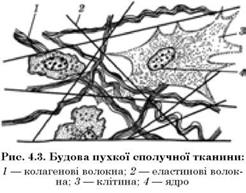
Пухка сполучна тканина — це сітчаста волокниста структура з міжклітинною речовиною. Вона входить до складу всіх тканин, органів, є між органами і в підшкірній клітковині. Крім волокон пухка сполучна тканина містить міжклітинну речовину з клітинами і ядрами. Деякі ділянки пухкої сполучної тканини містять значну частину жирових клітин (сальник, міжм’язовий жир) (рис. 4.3).
Щільна сполучна тканина містить розміщені щільно і паралельно товсті колагенові волокна. Вона є основою сухожиль м’язів, з’єднань суглобів, зв’язки і фасції.
Еластична сполучна тканина складається переважно з товстих еластинових волокон і входить до складу шийно- потиличної зв’язки, пахвини і кровоносних судин.
 Суха маса сполучної тканини містить до 40 % білків і до 30 % міжклітинної основної речовини.
Суха маса сполучної тканини містить до 40 % білків і до 30 % міжклітинної основної речовини.
Білкові речовини сполучної тканини.
Найхарактернішими компонентами сполучної тканини є специфічні білкові речовини, головним чином структурні білки-склеро- протеїни: колаген, еластин, ретикулін, що утворює міцні й еластичні волокнисті структури. Особливість білків цієї групи полягає в подовженій формі молекули, зумовленій паралельно розташованими поліпептидними ланцюгами. До складу елементарних речовин сполучної тканини входять специфічні білкові муцини і мукоїди, які відрізняються від інших склеропротеїнів за будовою і фі- зико-хімічними властивостями. У сполучній тканині в меншій кількості містяться також інші білки — альбумін, глобулін, нуклео- протеїди.
При нагріванні колаген з водою гідролізується на глютин і желатин. Він становить близько 30 % від усіх білків тваринного організму. Колаген входить до складу пухкої і щільної сполучної, кісткової, хрящової і покривної тканин, бере участь в утворенні сухожиль, зв’язок, фасцій.
Залежно від анатомічного походження колаген поділяють на волокнистий (у дермі і сухожиллях), гіаліновий (у кістковій тканині осеїн), хондриновий (у складі хрящів), іхтуліновий (у складі рибного міхура). Іхтуліновий колаген переходить у клей вже за температури 40 °С.
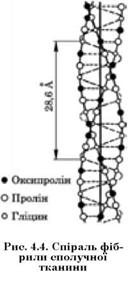
За допомогою електронної мікроскопії встановлено, що колагенові волокна побудовані із фібрил різного діаметра, які мають поперечне окреслення. Фібрили побудовані з макромолекул колагену — тропоколагену. Тропоколаген складається з трьох поліпеп- тидних ланцюгів, що утворюють потрійну спіраль діаметром близько 1,5 мм і завдовжки близько 300 мм. Кожен ланцюг складається з 1000 амінокислот і має молекулярну масу 1200. Структура макромолекули стабілізується водневими зв’язками між пептид- ними групами сусідніх ланцюгів. Особливості взаєморозташуван- ня молекул тропоколагену, зв’язаних кінець з кінцем і пліч-о- пліч, визначають характер будови фібрил (рис. 4.4). У результаті такої агрегації молекул тропоколагену утворюється четвертинна
структура колагену — протофібрили, що мають поперечне окреслення. Протофібри- ли об’єднуються у фібрили.
 Специфіка структури тропоколагену визначається особливістю його амінокислотного складу. Приблизно 33 % амінокислотних залишків макромолекул колагену становить гліцин, 21 % — пролін і оксипролін, 11 % — аланін. У колагені немає триптофану, цистину, цистеїну, мало метіоніну і тирозину.
Специфіка структури тропоколагену визначається особливістю його амінокислотного складу. Приблизно 33 % амінокислотних залишків макромолекул колагену становить гліцин, 21 % — пролін і оксипролін, 11 % — аланін. У колагені немає триптофану, цистину, цистеїну, мало метіоніну і тирозину.
Наявність у небагатьох білках оксипроліну дає змогу за вмістом цієї амінокислоти робити висновок про кількість колагену в м’ясі.
Особливості будови колагенових волокон визначають їх високу здатність до набухання і велику механічну міцність, що, в свою чергу, впливає на консистенцію м’яса. На- тивний колаген не розчиняється у воді, проте має здатність до набухання. Він стійкий до дії пепсину і трипсину, підлягає гідролізу в присутності колагенази підшлункової залози. Колаген може перетворюватися на легкозасвоювані поліпептиди у результаті гідролізу в присутності деяких рослинних ферментів. Під дією альдегідів відбувається дублення колагену, тобто утворення між пептид- ними ланцюгами метиленових містків, що підвищує його механічну міцність, стійкість при нагріванні в присутності води і впливу протеолітичних ферментів.
Теплове оброблення призводить до дезагрегації макромолекул колагену, характер яких залежить від температури і тривалості нагрівання.
За помірного теплового впливу колаген «зварюється» внаслідок порушення частини видимих зв’язків у середині пептидних ланцюгів. Зміни їх взаєморозташування у триспіральній структурі тропоколагену супроводжується її розпушенням, підвищенням гідратації системи і збільшенням доступних пептидних зв’язків дії протеаз.
Підвищення температури (до 90 °С) і збільшення тривалості нагрівання зумовлюють гідротермічний розпад тропоколагену на складові макромолекули — пептиди в результаті руйнування водневих зв’язків між ними. Продукт дезагрегації колагену — глютин — інтенсивно набухає у воді й за температури 40 °Спереходить у розчин, зниження температури якого супроводжується утворенням драглів.
Глютин легко перетравлюється протеолітичними ферментами. Подальше нагрівання за підвищених температур приводить до гідролізу пептидних зв’язків з утворенням низькомолекулярних
продуктів — глютоз (желатоз). При цьому може відбуватися їх взаємодія з утворенням нових сполук.
Наявність глютоз знижує гідратацію системи і негативно впливає на драглеутворення (знижується міцність драглів). Отже, характер змін колагену при тепловому обробленні м’ясної сировини може істотно впливати на якість готових виробів — їх консистенцію, водозв’язувальну здатність, перетравлюваність колагену ферментами травного каналу.
Еластин входить до складу еластинових волокон, що мають жовтувате забарвлення, які зовсім не подібні до колагенових. Вони безструктурні, здатні розгалужуватися і з’єднуватися між собою. Довжина еластинових волокон на відміну від колагенових при розтягуванні може збільшуватися вдвічі.
Еластинові волокна побудовані із сферичних молекул. Еластин — неповноцінний білок. Цей білок містить специфічні амінокислоти (десмозин і ізодесмозин), які беруть участь в утворенні поперечних зв’язків. Еластин дуже стійкий. Він не розчиняється в холодній і гарячій воді, має високу стійкість до дії кислот і лугів. На відміну від колагену він не змінюється під час нагрівання. Еластин не перетравлюється трипсином і хімотрипсином, але повільно гідролізується пепсином при рН 2,0. Продукована підшлунковою залозою еластаза, а також рослинні ферменти — фіцин, папаїн — зумовлюють протеоліз еластину.
За амінокислотним складом еластин дещо подібний до колагену завдяки наявності у ньому оксипроліну гліцину і проліну, дуже низькому вмісту гістидину, триптофану, цистеїну. Загальна частка гліцину, аланіну, валіну та проліну в еластині становить майже 70 % амінокислот.
На міжклітинну основну речовину припадає до 30 % сухої маси сполучної тканини. Зміна складу сполучної тканини залежить від віку тварин, що позначається на структурно-механічних властивостях сполучної тканини та її змінах під впливом зовнішніх факторів.
З фізіологічного і технологічного погляду наявність у м’ясі до 10 — 15 % сполучної тканини є позитивним.
У ковбасному і консервному виробництві колагенвмісну сировину найефективніше можна використовувати у вигляді білкових стабілізаторів, емульсій або як попередньо облагороджений компонент рецептур низькосортних м’ясних виробів, переважно із субпродуктів.
