4.12.3. Хімічний склад і властивості формених елементів крові
Залежно від виду тварин в 1 мм3 міститься 200 — 600 тис. тромбоцитів, 6 — 8 млн еритроцитів; у крові ВРХ 7 — 9 тис. лейкоцитів, свиней — 6 — 12 тис., ДРХ — 9 — 16 тис., коней — 8 —11 тис.
Еритроцити ссавців циркулюють у потоці крові, не маючи ядра. Більшість сільськогосподарських тварин мають еритроцити круглої приплюснутої форми в природних умовах ізотонії.
Червоний колір еритроцитів зумовлений наявністю в них білка гемоглобіну. Гемоглобін міститься в середині еритроциту, який має ліпоїдно-білкову природу, тому його основа (строма) є губчастою.
Ущільнена строма утворює на поверхні еритроциту оболонку, проникну для води, моносахаридів, сечовини і аніонів, але не проникну для катіонів. При порушенні осмотичного тиску між плазмою і еритроцитами, механічному пошкодженні або розбавлянні крові водою порушується цілісність оболонки еритроциту, внаслідок цього глобін переходить у плазму і, розчиняючись, надає їй інтенсивнішого червоного кольору. Це явище називають гемолізом.
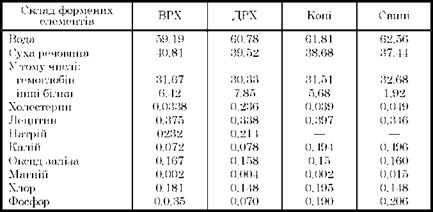
Масову частку формених елементів у крові тварин наведено в табл. 4.18.
|
Таблиця 4.18. Масова частка формених елементів у крові тварин, г/100 г формених елементів
|
Гемоглобін належить до складних білків (хромопротеїдів) і має молекулярну масу 68 000. Характерною особливістю гемоглобіну є наявність простого білка глобіну і простатичної небілкової залізовмісної групи — гему.
Одна молекула гемоглобіну містить чотири атоми заліза і відповідно чотири геми. Характерною особливістю гемоглобіну є його здатність зв’язувати кисень (оксигемоглобін) і не менш легко його віддавати без зміни валентності. Так, 100 г гемоглобіну може зв’язати 134 мл кисню при 0 °С і тиску 101 080 Па.
Гемоглобін, який не зв’язаний з киснем і містить гем з феро- іоном (Ее2+), називають дезоксигемоглобіном, ферогемоглобіном або відновленим гемоглобіном і скорочено позначають НЬ. Атоми заліза кожної з гем-груп молекули гемоглобіну можуть зворотно зв’язувати молекулу кисню О2. Повністю насичений киснем гемоглобін НЬ називають оксигемоглобіном (НЬО2) і містить чотири молекули кисню на молекулу гемоглобіну. Гемоглобін може також з’єднуватися з чотирма молекулами СО з утворенням СО-гемо- глобіну або карбоксигемоглобіну НЬСО. До молекулярного гемоглобіну можуть приєднуватися чотири молекули N0 з утворенням стабільного №N0.
Взаємодія Hb з пероксидами, фераціанідами і хінонами може призводити до окиснення Fe2+ в Fe3+ з утворенням метміоглобіну (MetHb), який не приєднує О2 і СО і для зворотної реакції потребує впливу сильних відновників, наприклад гідросульфату натрію
(Na2S204).
Гемоглобін дисоціює на гем і глобін у кислому або лужному середовищі. Так, якщо розчин Hb додати до суміші ацетон — HCl, то гем залишиться в розчині, а глобін випаде в осад:
Гемоглобін + HCl ^ глобін-HCl + феропротопорфірин.
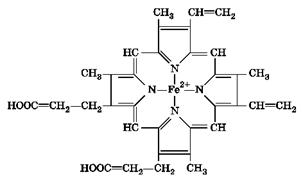
Гемоглобін складається з двох пар нековалентних пептидних ланцюгів, які, поєднуючись, утворюють глобулярну нативну молекулу. В цій молекулі з кожним ланцюгом зв’язана одна гем-група, розміщена (укладена) в гідрофобні глобінові кармани молекули глобіну (рис. 4.9). У гідрофобних карманах створюються умови низької діелектричної дисоціації, що дає змогу кисню О2 реагувати з гемовою групою без окиснення Fe2+ в Fe3+, не розділяючи зарядів у комплексі гєм^є2+-"О2 з утворенням гем-Fe^ + 02, внаслідок чого кисень зв’язується зворотно без окиснення гемового заліза.
|
Рис. 4.9. Простетична залізовмісна група — феропротопорфірин (гем) |
У розчинах з високою діелектричною дисоціацією кисень![]() реагує з вільним ферогемом, що зумовлює утворення ферігему і су- пероксидного іону
реагує з вільним ферогемом, що зумовлює утворення ферігему і су- пероксидного іону![]() за реакцією
за реакцією
![]()
За своєю третинною структурою гемоглобін НЬ дуже подібний до міоглобіну м’язів ссавців, що як оксиміоглобін![]() є депо
є депо![]()
у м’язах тварин.
У крові тварин виокремлюють два основних класи лейкоцитів: поліморфноядерні лейкоцити і лімфоцити.
За хімічним складом неорганічних іонів лейкоцити і еритроцити майже не відрізняються, проте лейкоцити мають в 25 разів більше цинку і організовану систему дихальних і гліколітичних ферментів.
Поліморфноядерні лейкоцити містять глікоген, кількість якого залежить від вмісту глюкози в крові тварин.
Лімфоцити — це лімфоїдні клітини, які містять білок, ідентичний у-глобуліну плазми крові, і відіграють важливу роль у синтезі білка і особливо в утворенні антитіл імуномодуляторів.
Плазму і сироватку крові при виробництві ковбасних виробів використовують для заміни свинини та яловичини (3 кг сироватки замінюють 1 кг яловичини). Під час виробництва пельменів замість 50 % меланжу беруть сироватку.
У вирішенні проблеми раціонального використання продуктів забою значна роль належить організації збирання та первинної переробки крові забійних тварин.