2.1. Теоретичні основи процесу екстрагування
Основною стадією виробництва фітопрепаратів є екстрагування рослинної сировини, обумовлене загальними законами масоперсдачі, властивостями рослинної клітини й фізико-хімічною спорідненістю екстрагенту й речовин, що витягуються. Екстракція являє собою складний процес, який включає діаліз, десорбцію, розчинення й дифузію, що протікають довільно й одночасно, як один загальний процес.
Для одержання витягу екстрагент повинен проникнути усередину клітин рослинної сировини, які мають клітинні перегородки. У свіжій сировині жива рослинна клітина має пристінковий шар протоплазми, який робить стінку клітини напівпроникною, що не пропускає назовні розчинені в клітинному соку речовини. Тому при одержанні витягів зі свіжих рослин клітини убивають етиловим спиртом, який, знезводню- ючи клітину, викликає найсильніший плазмоліз.
Вихідною сировиною для більшості препаратів служать висушені частини рослин, у яких діючі речовини перебувають у вигляді сухих конгломератів, адсорбованих на стінках клітини й у порах При висушуванні відбувається загибель протоплазми: клітинна стінка втрачає властивості напівпроникної мембрани й починає пропускати речовини в обидва боки, тобто набуває властивостей пористої перегородки. Наявність пористої перегородки знижує швидкість дифузійних процесів. Через пори перегородки можуть пройти тільки ті речовини, частки яких не перевищують розміри пор. Крім того, використовувані подрібнені частини рослин мають різну клітинну структуру й складаються з розчинних і нерозчинних речовин.
Процес екстрагування висушеної сировини можна розділити на кілька стадій.
Витягування починається із проникнення екстрагенту усередину часточок рослинного матеріалу спочатку по макро-, потім по мікротрі- щннах, по міжклітинних ходах, порах, численних капілярах, заповнюючи клітини й інші порожнечі в сировині. Проникнення екстрагенту всередину клітини, тобто рух екстрагенту через пористу перегородку, має назву ендоосмосу. Час заповнення капілярів рідиною може бути досить тривалим, тому що заповненню заважає повітря, яке перебуває в рослинній тканині. Для прискорення заповнення капілярів застосовують вакуумування, підвищення тиску рідини, заміну повітря на легкорозчинний газ.
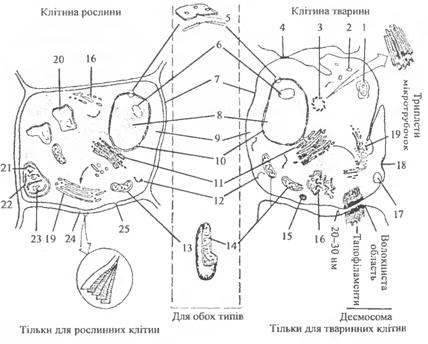
При проникненні екстрагенту в сировину одночасно відбувається й процес змочування речовин, що перебувають усередині клітин (рис. 2.1). Ефективність змочування речовин екстрагентом залежить від спорідненості речовин (гідрофільні й гідрофобні) і екстрагенту. Оболонки клітин володіють діфільними властивостями з перевагою гідрофільності. Чим більша спорідненість екстрагенту до матеріалу, тим він швидше змочує стінки капілярів і проникає в сировину. Змочування й проходження екстрагенту по капілярах поліпшується при введенні в екстрагент ПАР, які знижують поверхневий натяг на межі поділу фаз і гідрофілізують гідрофобні фрагменти сировини.
Процес розчинення біологічно активних речовин, які знаходяться на клітинних стінках у вигляді сухих фрагментів матеріалу, називають стадією утворення «первинного соку». Усередині клітин екстрагент взаємодіє з речовинами, синтезованими органоїдами клітин, що перебувають у цитоплазмі (ядро, мітохондрії, рибосоми, ендоплазматична мережа, комплекс Гольджі й ін.): вони розчиняються, а необмежено набухаючі ВМС набухають і пептизуються (десорбція й розчинення); обмежено набухаючі ВМС набухають, утворюючи драглі. Усередині кліток утворюється концентрований розчин розчинних речовин - «первинний сік». Швидкість виходу розчинних речовин визначається швидкістю їх масоиередачі: спочатку в екстрагент міжклітинного простору, потім в екстрагент, що омиває сировину; а на поверхні часток (при зруйнованих клітинах і відкритих порах) - швидкістю масовіддачі від поверхні тіла.
|
Рис. 2.1. Будова еукаріотичної клітини: 1 - лізосома, 2 - жирова крапля, 3 - цен- тріоля, 4 щільний контакт, 5 - ядерні нори, 6 - ядерце, 7 - плазматична мембрана (як у прокаріотів), 8 - конденсований хроматин, 9 - цитоплазма, 10 - ядро, 11 — шорсткий ендоплазматичний ретикулум, 12 - рибосоми (і полірибосоми), 13 — мітохондрії, 14-кристи, 15 облямований пухирець. 16 - гладенький ендоплазматичний регикулум, 17 - піноцитозний пухирець, 18 - облямована ямка, 19 - комплекс Гольджі, 20 - вакуоля, 21 — фотосинтезуючі ламели, 22 - хлоропласт, 23 - ДНК, 24 - клітинна стінка (шари целюлози), 25 - плазмодесма |
Масопереиос здійснюється за допомогою скзоцитозу й єндоцитозу речовин через пористі клітинні стінки всередині рослинної сировини. Він складається із процесів вільної молекулярної дифузії в клітинному соку (розчині) і внутрішньої дифузії через клітинні мембрани. Швидкість масопереносу через мембрану при цьому залежить від товщини й кількості шарів мембрани, кількості й діаметра пор, які коливаються в широких межах залежно від виду сировини.
Вільна молекулярна дифузія обумовлена хаотичним рухом молекул, що межують одна з одною і перебувають у макроскопічному спокої. Швидкість дифузії збільшується при підвищенні температури, тому що при цьому зростає швидкість руху молекул. Рушійною сплою дифузійного процесу є річниця концентрацій розчинених речовин у стичних рідинах. На швидкість дифузії впливають: відносна молекулярна маса речовини товщина шару, через який відбувається дифузія, площа поверхні поділу й час дифузії.
Швидкість молекулярної вільної дифузії математично виражається першим законом Фіка:
|
|
Масопереиос речовин від поверхні рослинного матеріалу в розчин є останньою стадією процесу екстрагування. У результаті високої концентрації «первинного соку» всередині клітини створюється значний осмотичний тиск, що викликає дифузійний обмін між вмістом клітин і рідиною, що їх оточує, з меншим осмотичним тиском. Спочатку із клітин дифундують більш рухливі молекули з меншою молекулярною масою. Повільніше дифундують складні високомолекулярні речовини. Найменша швидкість дифузії у колоїдних компонентів.
Відповідно до теорії дифузійного шару механізм цього процесу наступний. На поверхні сировини є пристінковий шар екстрагенту, у який переходять речовини з гіор рослинного матеріалу. Швидкість масопе- реносу значною мірою залежить від говшини цього дифузійного пограничного шару, яка постійно міняється залежно від руху екстрагенту.
При енергійному перемішуванні пограничний шар зменшується й переходить у дифузійний підшар. Молекулярна дифузія заміняється конвективною при турбулентному потоці рідини, коли товщина прикордонного шару може стати рівною нулю.
Конвективна дифузія - це перенос речовини у вигляді невеликих об’ємів її розчину рухомим екстрагентом. Цей вид дифузії значно швидший і відбувається в результаті перемішування, вібрації, підвищення температури, тобто причин, що викликають переміщення ріди ни, а разом з нею - розчиненої речовини в турбулентному потоці. При конвективній дифузії розмір молекул речовини, що дифундує, в’язкість розчинника, кінетична енергія молекул стають другорядними. Головними для швидкості конвективногопереносу речовини стають гідродинамічні умови (швидкість і режим руху рідини). Зазвичай швидкість конвективного переносу незрівнянно більша від швидкості молекулярного переносу.
Швидкість конвективно!’ дифузії можна виразити рівнянням:
![]()
де![]() - коефіцієнт конвективної дифузії, що характеризує швидкість масопереносу в рухомому шарі екстрагенту, що омиває сировину.
- коефіцієнт конвективної дифузії, що характеризує швидкість масопереносу в рухомому шарі екстрагенту, що омиває сировину.
Конвективная дифузія може бути природною (довільною), яка відбувається за рахунок різниці густин екстрагенту й розчину, зміни температури й гідростатичного тиску стовпа рщини, а також примусовою, котра виникає при перемішуванні мішалками, насосами, вібрацією і т.д. Конвективна дифузія сприяє інтенсифікації процесу масообміну.
Таким чином, процес екстракції рослинної сировини характеризується трьома видами масопереносу:
1) «внутрішньою» дифузією (масоперенос усередині часток рослинної сировини), кількісно оцінюваною коефіцієнтом Dвм;
2) масопереносом у клітинному соку й пограничному дифузійному шарі, кількісно оцінюваним коефіцієнтом D;
3) масопереносом у рухомому шарі екстрагенту (конвективна дифузія), кількісно оцінюваним коефіцієнтом р.
Фактори, що виливають на ефективність процесу екстрагування
Для приготування витягів використовують різні частини висушених лікарських рослин: траву, листя, кору, коріння, кореневища, бруньки, плоди.
Кількість діючих речовин у рослинній сировині залежить від: часу збору, режиму сушіння, умов зберігання й інших факторів. Сировина, використовувана для готування витягів, повинна бути стандартною, тобто відповідати вимогам АНД по зовнішньому вигляду, кількості діючих речовин, подрібненості, вологості, кількості допустимих домішок, радіологічному контролю. Кількість діючих речовин вказується у сертифікаті якості сировини, що додається до рослинної сировини, або у відсотках (алкалоїди, ефірні олії й ін.) чи в біологічних одиницях (ОД, ЖОД, КОД) на 1 г сировини (глікозиди). Сировина, що містить занижену кількість діючих речовин, використовуватися не повинна. При використанні сировини з підвищеним вмістом діючих речовин варто зробити перерахунок її кількості:
|
|
де X — кількість сировини, яку необхідно взяти з урахуванням завищеного вмісту діючих речовин, г; а — необхідна кількість стандартної сировини, г; с — кількість діючих речовин у даній сировині; b — стандартна концентрація діючих речовин у тих самих одиницях.
При виробництві екстракційних препаратів з рослинної сировини, які прийнято називати галеновими й новогаленовими (максимально очищеними), важливе значення має доброякісність сировини (А), що являє собою відношення вмісту діючих речовин (а) до кількості екстрактивних речовин![]() - і доброякісність препаратів (А^, приготовлених із природної сировини без додавання наповнювачів, що являє собою відношення вмісту діючих речовин (а) до сухого залишку (с):
- і доброякісність препаратів (А^, приготовлених із природної сировини без додавання наповнювачів, що являє собою відношення вмісту діючих речовин (а) до сухого залишку (с):![]()
Поверхня поділу фаз![]() — «тверде тіло — рідина» залежить від ступеня подрібнення сировини й буде тим більша, чим менші її часточки.
— «тверде тіло — рідина» залежить від ступеня подрібнення сировини й буде тим більша, чим менші її часточки.
Однак з пракгики відомо, що при занадто тонкому подрібнюванні сировина може злежуватися, а при вмісті слизуватих речовин — ослиз- нятися, а через такі маси проходження екстрагенту утруднюється, що призводить до неповного екстрагування БАР.
При занадто тонкому подрібнюванні різко збільшується кількість розірваних клітин, що призводить до вимивання супутніх речовин, які забруднюють витяжку (білки, слизи, пектини й інші високомолекуляр- ні сполуки). У результаті витяжки виходять мутні, важко освітлюються й погано фільтруються. Тому крупну сировину варто подрібнювати до оптимальних розмірів: листя, квіти, трави - до 3-5 мм; стебла, корені, кору — до 1—3 мм, плоди й насіння — до 0,3—0,5 мм.
Різниця концентрацій у сировині СІ і екстрагенті С2 є рушійною силою процесу екстракції. Під час екстракції необхідно прагнути до максимального перепаду концентрацій, що досягається частішою зміною екстрагенту (ремацерація, замість мацерації), проведенням проти- течійного процесу, створенням динамічних умов екстрагування.
Час (тривалість) екстрагування. З основного рівняння масопере- дачі випливає, що кількість речовини, яка продифундувала через деякий шар, прямо пропорційна часу екстракції.
Надмірна тривалість процесу екстрагування призводить до забруднення витяжок супутніми високомолекулярними сполуками, швидкість дифузії яких значно менша, ніж у біологічно активних речовин, що під впливом ферментів призводить до протікання небажаних процесів.
В ’язкість екстрагенпп'. За законом Фіка кількість розчиненої речовини, яка продифундувала через деякий шар екстрагенту, зворотньо пропорційна в’язкості цього екстрагенту при даній температурі. Отже, менш в’язкі розчини мають більшу дифузійну здатність. Для зменшення в’язкості екстрактів при екстрагуванні рослинними оліями використовують нагрівання.
Температура. Підвищення температури прискорює процес екстрагування, але в умовах фітохімічних виробництв підігрів використовують тільки для водних витягів. Спиртова й тим більше ефірна екстракція проводиться при кімнатній (або нижчій) температурі, оскільки з її підвищенням збільшуються втрати екстрагентів, а отже, зростає шкідливість і небезпека роботи з ними.
Добавка поверхнево-активних речовин (ПАР). Експериментально встановлено, що додавання невеликих кількостей ПАР (0,01—0,1 %) по-
ліпшує процес екстрагування. При цьому збільшується кількість екстрагованих речовин - алкалоїдів, глікозидів, ефірних олій та інших, а в деяких випадках повнота екстрагування досягається при меншому об’ємі екстрагенту. Добавки ПАР знижують поверхневий натяг на межі поділу фаз, поліпшуючи змочуваність вмісту клітини і полегшуючи проникнення екстрагенту. Крім гого, істотну роль відіграє солюбілізу- юча здатність ПАР (твінів, спенів та ін.).
Вибір екстрагенту. Для забезпечення повноти екстракції діючих речовин і максимальної швидкості екстрагування до екстрагенту висувають наступні вимоги: селективність (вибіркова розчинність); хімічна й фармацевтична індиферентність; мала токсичність; доступність.
Вибір екстрагенту визначається ступенем гідрофільності речовин, які екстрагують. Для витягування полярних речовин з високим значенням діелектричної постійної використовують полярні розчинники: воду, метанол, гліцерин; для неполярних — кислоту оцтову, хлороформ, ефір етиловий та інші органічні розчинники. Найчастіше в якості екстрагенту застосовують етанол — малополярний розчинник, який при змішуванні з водою дає розчини різного ступеня полярносг,, що дозволяє використовувати його для вибіркового екстрагування різних біологічно активних речовин Крім етанолу, з малополярних розчинників застосовують ацетон, пропанол, бутанол.
Пористість і порозність сировини. Пористість сировини — цс сумарна площа порожнеч усередині рослинної тканини. Чим вона вища, тим більше утворюється внутрішнього соку при набряканні. Порозність - це сума» і а площа порожнеч між шматочками подрібненого матеріалу. Від величини пористості й порозності залежить швидкість змочування й набрякання матеріалу. Швидкість набрякання зростає при попередньому вакуумуванні сировини, а також при підвищенні тиску й температури.
Пористість і порозність сировини обумовлює її поглинаючу здатність, яка характеризується коефіцієнтом поглинання сировини Ка.
![]()
де Р] і Р, - маса сировини відповідно до й після набрякання.
Поглинаюча здатність сировини перебуває в прямій залежності від ступеня її подрібнювання
Коефіцієнт вимивання. Характеризує ступінь зруйнованих клітин у подрібненій сировині. Якщо він низький, це значить, що в сировині мало зруйнованих клітин, екстрагування йде повільно й визначається в основному швидкістю молекулярної дифузії. За величину коефіцієнта вимивання приймають кількість речовин у витяжці, отриману з певної наважки сировини, при певному співвідношенні „сировина —екстрагент”, при екстрагуванні сировини протягом однієї години при певній швидкості перемішування.
Вшив вібрацій, пульсацій, подрібнювання и деформації сировини в середовищі екстрагенту. Використання методів екстрагування, у яких мають місце вібрації, пульсації, подрібнювання й деформація в середовищі екстрагенту, дозволяє значно збільшити швидкість і повноту екстрагування БАР із сировини.
Внаслідок появи турбулентного перемішування як усередині, так і зовні клітин молекулярно-кінетичний рух заміняється конвсктивним, що дозволяє підтримувати різницю концентрацій у зоні зіткнення фаз на високому рівні.
Вплив ел ектро іл і пул ьсних розрядів. При екстрагуванні за допомогою електричних розрядів прискорюється процес витягу БАР, тому що через іскровий розряд у сировині відбувається мікровибух, який руйнує клітинні структури матеріалу.
Вимоги до екстрагентів
Екстрагент у процесі екстракції БАР відіграє особливо важливу роль. Він повинен мати здатність проникати через стінки клітини, вибірково розчиняти біологічно активні речовини, а також сприяти їх виходу за межі рослинного матеріалу. Екстрагент підбирається відповідно до природи діючих речовин у сировині й залежить від ступеня їх гідрофільності.
Речовини гідрофільні — солі алкалоїдів, глікозиди, дубильні речовини - добре розчинні в полярних розчинниках, характеризуються високим значенням діелектричної сталої (табл. 2.1) і, отже, добре витягуються ними. Речовини змішаної групи розчинні в малополярних розчинниках, а гідрофобні речовини (жирні й ефірні олії, жиророзчинні вітаміни, смоли і т.д.) — у неполярних розчинниках, які мають низьку величину діелектричної сталої. Екстрагент впливає не тільки на витяг якоїсь певної групи речовин, але й на загальну кількість екстрагованих речовин.
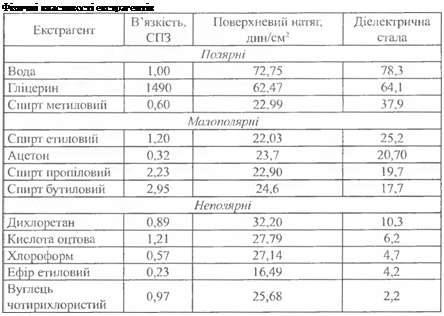
 Таблиця 2.1
Таблиця 2.1
Екстрагент повинен володіти:
- вибірковістю, тобто максимально розчиняти лікарські речовини, і мінімально — баластові речовини;
- високою змочувальною здатністю, що забезпечує проникнення його через пори матеріалу й стінки клітин; здатністю перешкоджати розвитку у витяжці мікрофлори;
- леткістю, по можливості низькою температурою кипіння, здатністю легко регенеруватися;
- мінімальною токсичністю й вогненебезпечністю;
- бути доступним за вартістю.
Із двох рівноцінних екстрагентів вибирають менш вогненебезпечний, доступніший за ціною, фармакологічно менш шкідливий і т.д. Якщо ж екстрагент не задовольняє зазначені вимоги, то застосовують суміші, наприклад, підкислену воду, спирт із водою, ефір зі спиртом і т.п.
Найчастіше застосовуються як екстрагенти: вода, спирт етиловий, ацетон, ефір діетиловий, хлороформ, дихлоретан, метилен хлористий, метанол (спирт метиловий), олії рослинні.
Перспективними для екстрагування є пропоновані останнім часом зріджені гази: вуглецю діоксид, пропан, бутан, рідкий аміак, хладони (хлорфторпохідні вуглеводнів) та ін. Зріджений вуглецю діоксид добре витягує ефірні олії, жирні олії й інші гідрофобні речовини. Гідрофільні речовини добре екстрагуються зрідженими газами з високою діелектричною проникністю (аміак, метил хлористий, ме- тиленоксид та ін.).
Екстрагування зрідженими газами проводиться під тиском, при знятті якого екстрагент звітрюється, а екстрактивні речовини залишаються в чистому вигляді.